Лечение неврологических нарушений
Тут будет переклад українською...
Фармакологическое действие Противоэпилептическое средство, производное трициклического иминостильбен
Фармакологическое действие Противоэпилептическое средство, относится к классу сульфат-замещенных мон
Тут будет переклад українською...
Фармакологическое действие Противоэпилептический препарат. Топирамат относится к сульфат-замещенным
Фармакологическое действие Противоэпилептический препарат, производное пирролидона (S-энантиомер ?-э
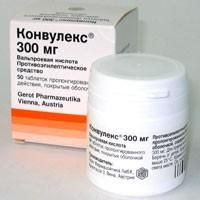
КонвулексФорма выпускаКапсулыСостав1 капс. содержит вальпроевая кислота 300 мг, вспомогательные веще
Фармакологическое действие Противоэпилептическое средство, относится к классу сульфат-замещенных мон
Фармакологическое действие Натрия вальпроат увеличивает содержание GABA (гамма-аминобутировой кислот
КонвулексФорма выпускаТаблеткиСоставВальпроат натрия.Вспомогательные вещества: моногидрат лимонной к
Тут будет переклад українською...
Фармакологическое действие Противосудорожное средство. Механизм действия связан с влиянием на потенц
Фармакологическое действие Противоэпилептический препарат. Стабилизирует потенциал-зависимые натриев
Фармакологическое действие Противосудорожный препарат. Натрия вальпроат повышает содержание гамма-ам
Фармакологическое действие Габагамма - противоэпилептический препарат. Габапентин по строению с
Фармакологическое действие Противоэпилептический препарат, производное пирролидона (S-энантиомер аль
Фармакологическое действие Противоэпилептическое средство, производное трициклического иминостильбен
Тут будет переклад українською...
Тут будет переклад українською...
Карбалепсин ретардФорма выпускаТаблеткиСоставАктивное вещество: карбамазепин 200 мг Вспомогательные
Тут будет переклад українською...
ТопсаверЛатинское названиеTopsaverФорма выпускаБелые, круглые, двояковыпуклые таблетки, покрытые пле
Фармакологическое действие Противоэпилептический препарат, производное пирролидона (S-энантиомер ?-э
Фармакологическое действие Противосудорожный препарат. Натрия вальпроат повышает содержание гамма-ам