- Головна
- Лекарства и БАДы
- Лечение заболеваний дыхательной системы
Лечение заболеваний дыхательной системы Алмирал С.А.
Сортувати по:
Фільтр
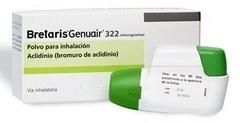
1 980,60 грн
1 923,60 грн
Фармакологическое действие Аклидиния бромид является конкурентным, селективным антагонистом мускарин
1 141,60 грн
1 095,60 грн
Фармакологическое действие Аклидиния бромид является конкурентным, селективным антагонистом мускарин